遠(yuǎn)大醫(yī)藥(0512.HK)重磅核藥SIR-Spheres®釔[90Y]微球注射液(易甘泰®)再度迎來里程碑進(jìn)展��!
4月13日,遠(yuǎn)大醫(yī)藥發(fā)布公告稱����,公司釔[90Y]微球注射液在美國開展的用于治療不可切除肝細(xì)胞癌(HCC)臨床研究(DOORwaY90研究)已成功達(dá)到預(yù)設(shè)臨床終點,取得了亮眼的臨床數(shù)據(jù)����。優(yōu)異的臨床數(shù)據(jù)不僅標(biāo)志著SIR-Spheres個體化劑量學(xué)治療模式超越了傳統(tǒng)治療方案,更進(jìn)一步拓寬了不可切除HCC患者肝臟定向治療的應(yīng)用空間��,同時也充分體現(xiàn)了產(chǎn)品強大的療效與市場潛力��,有望進(jìn)一步促進(jìn)遠(yuǎn)大醫(yī)藥釔[90Y]微球注射液在全球市場自主銷售的持續(xù)高速放量�����。
圖片由客戶提供
值得一提的是���,此前美國FDA已基于DOORwaY90臨床試驗的突破性中期數(shù)據(jù)����,正式批準(zhǔn)釔[90Y]微球注射液用于不可切除肝細(xì)胞癌適應(yīng)癥�,使其成為獲FDA批準(zhǔn)用于不可切除HCC和結(jié)直腸癌肝轉(zhuǎn)移雙重適應(yīng)癥的選擇性內(nèi)放射治療產(chǎn)品。此次DOORwaY90研究達(dá)成臨床終點,不僅為釔[90Y]放射栓塞療法作為不可切除HCC高效且兼具肝臟保護(hù)作用的確定性治療方案提供了堅實的臨床證據(jù)��,相關(guān)臨床數(shù)據(jù)也將為其在中國適應(yīng)癥拓展提供有力支持�����。同時�����,該成果也彰顯了遠(yuǎn)大醫(yī)藥優(yōu)異的海外臨床注冊能力��,為后續(xù)自研創(chuàng)新核藥產(chǎn)品的海外研發(fā)與注冊推進(jìn)奠定重要基礎(chǔ)�。
臨床研究數(shù)據(jù)喜人����,適應(yīng)癥拓展促進(jìn)市場空間戰(zhàn)略性擴(kuò)容
根據(jù)公告,釔[90Y]微球注射液是一款針對肝臟惡性腫瘤的選擇性內(nèi)放射治療產(chǎn)品�����,采用介入技術(shù)將釔[90Y]樹脂微球注入肝臟腫瘤血管�,釋放高能量β放射線殺滅腫瘤細(xì)胞,兼具了放射性藥物和精準(zhǔn)介入治療的雙重優(yōu)勢��。
實際上��,釔[90Y]微球注射液已是一款經(jīng)過長期市場與臨床雙重檢驗的成熟重磅產(chǎn)品,上市二十多年來�,該產(chǎn)品憑借穩(wěn)定可靠的表現(xiàn),已經(jīng)在50多個國家和地區(qū)應(yīng)用���,累計使用超過15萬人次���,其療效與安全性得到全球醫(yī)生與患者的廣泛認(rèn)可,并被美國國立綜合癌癥網(wǎng)絡(luò)(NCCN)等多個國際機構(gòu)的治療指南推薦�,同時也進(jìn)入了《原發(fā)性肝癌診療指南(2026年版)》等多項中國的臨床實踐指南。在國內(nèi)市場����,易甘泰®更是展現(xiàn)出巨大的商業(yè)化實力,帶動遠(yuǎn)大醫(yī)藥核藥抗腫瘤診療板塊四年內(nèi)收入增長近15倍�。基于遠(yuǎn)大醫(yī)藥在海外的自主銷售網(wǎng)絡(luò)��,憑借此次臨床數(shù)據(jù)的強力加持�����,未來釔[90Y]微球注射液海外銷售有望進(jìn)一步提升���。
此次釔[90Y]微球注射液DOORwaY90臨床試驗是美國頭個采用分割劑量學(xué)技術(shù)對不可切除HCC患者實施90Y選擇性內(nèi)放射治療(SIRT)的關(guān)鍵性��、前瞻性��、多中心臨床研究��。研究數(shù)據(jù)顯示�����,本次研究已成功達(dá)到預(yù)先設(shè)定的共同主要終點����,臨床數(shù)據(jù)極為亮眼——經(jīng)盲法獨立中心審查評估,完全緩解率(CR)高達(dá)90%����,最佳總體緩解率(ORR)為99%�;所有可評估患者均對治療產(chǎn)生應(yīng)答,局部腫瘤控制率達(dá)到100%��,這是90Y治療中迄今報道的高應(yīng)答療效之一��;同時����,釔[90Y]微球注射液也展現(xiàn)了持久的治療效果�,75%的患者緩解持續(xù)時間超過6個月����,中位緩解持續(xù)時間達(dá)到295天,超過95%的患者在12個月時維持了穩(wěn)定的肝功能��。
優(yōu)異的臨床研究數(shù)據(jù)表明����,釔[90Y]微球注射液能夠在不損傷肝臟儲備功能的前提下實現(xiàn)腫瘤應(yīng)答,有望改寫HCC診療格局�����,為患者帶來更長生存期及更高生活質(zhì)量��。同時���,釔[90Y]微球注射液個體化劑量學(xué)治療模式不僅超越了傳統(tǒng)治療方案��,更進(jìn)一步拓寬了不可切除HCC患者肝臟定向治療的應(yīng)用空間�,為患者提供更為精準(zhǔn)的治療方案����。此次臨床研究圓滿達(dá)到預(yù)設(shè)終點��,將有力支撐釔[90Y]微球注射液適應(yīng)癥范圍進(jìn)一步拓展�,直接推動產(chǎn)品市場空間實現(xiàn)戰(zhàn)略性擴(kuò)容�。
肝癌是第六大新發(fā)癌癥以及第三大致死癌癥。根據(jù)GLOBOCAN 2022年的數(shù)據(jù)���,肝癌全球新發(fā)病例約87萬����,死亡病例約76萬��。中國國家癌癥中心2024年全國癌癥報告顯示���,2022年中國新發(fā)肝癌約37萬例(占全球42.5%)�����,居腫瘤第四位;死亡病例約32萬例(占全球42.1%)��,居第二位���。
在所有肝癌類型中�,肝細(xì)胞癌(HCC)常見,占比高達(dá) 85%–90%�。但肝癌早期癥狀隱蔽,很難及時發(fā)現(xiàn)�,導(dǎo)致不足30%的患者在初次確診時能夠接受根治性手術(shù)。即便完成手術(shù)切除�����,術(shù)后5年復(fù)發(fā)轉(zhuǎn)移率仍高達(dá) 50%–70%�。從生存結(jié)果來看,中國肝癌患者5年生存率僅為12%�,臨床存在巨大未被滿足的治療需求。數(shù)據(jù)顯示����,2030年全球肝癌治療藥物市場規(guī)模預(yù)計將達(dá)到約98.1億美元,此外�����,在中國HCC藥物市場空間預(yù)計將于2030年達(dá)到約487億元人民幣��,市場空間非?����?捎^。
釔[90Y]微球注射液臨床的優(yōu)異表現(xiàn)�����,為中晚期肝癌患者提供了高效��、可及�、耐受性更好的治療選擇。隨著該產(chǎn)品美國臨床成功����,其全球商業(yè)化爆發(fā)將獲得更加強力的數(shù)據(jù)支持,未來不僅有望更快�、更廣地惠及國內(nèi)患者,助力提升我國肝癌整體診療水平��,同時也將為全球患者提供更優(yōu)的治療選擇��,進(jìn)一步促進(jìn)遠(yuǎn)大醫(yī)藥核藥板塊的高速增長�����。
全鏈布局全球�����,持續(xù)加固核藥全產(chǎn)業(yè)鏈壁壘優(yōu)勢
釔[90Y]微球注射液美國關(guān)鍵臨床圓滿達(dá)成終點���,不僅進(jìn)一步驗證了產(chǎn)品的療效�,更體現(xiàn)了遠(yuǎn)大醫(yī)藥雄厚的海外研發(fā)注冊能力�。在核藥領(lǐng)域,公司以波士頓�、成都為核心的研發(fā)基地,波士頓����、法蘭克福、新加坡�、成都所在的生產(chǎn)基地以及覆蓋全球50多個國家和地區(qū)的自主銷售網(wǎng)絡(luò)為基礎(chǔ),已構(gòu)建起覆蓋研發(fā)���、生產(chǎn)��、配送���、銷售的全鏈條全球化體系——公司在海外具備強大的自主研發(fā)注冊和商業(yè)化能力,已成為全球核藥抗腫瘤領(lǐng)域企業(yè)���。
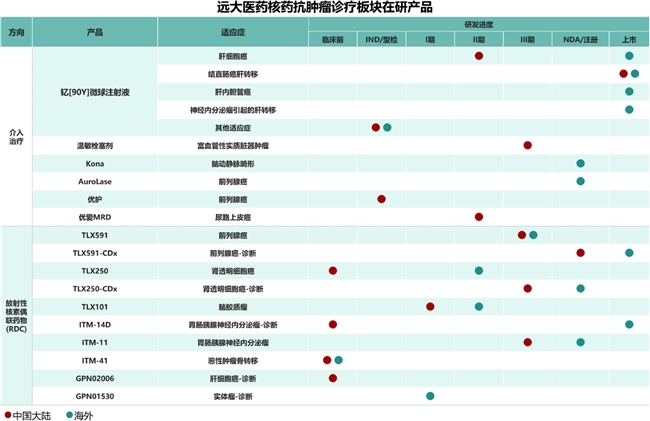
在產(chǎn)品管線方面�����,遠(yuǎn)大醫(yī)藥堅持“診療一體化”發(fā)展理念��,構(gòu)建多層次�����、高質(zhì)量創(chuàng)新矩陣�。目前公司在研發(fā)注冊階段已布局16款創(chuàng)新核藥產(chǎn)品,涵蓋68Ga���、177Lu��、131I�����、90Y���、89Zr在內(nèi)的5種關(guān)鍵放射性核素,覆蓋肝癌、前列腺癌���、腎癌、腦癌等7大癌種�����;早期研發(fā)階段儲備10余款藥物��,形成診斷與治療協(xié)同��、多適應(yīng)癥覆蓋的良好格局����。目前,公司已有6款創(chuàng)新RDC藥物進(jìn)入注冊臨床研究�,其中1款已進(jìn)入NDA階段,3款已進(jìn)入III期臨床階段����,創(chuàng)新核藥管線潛力巨大。
圖片由客戶提供
近年來�,遠(yuǎn)大醫(yī)藥核藥板塊核心產(chǎn)品與重磅管線接連實現(xiàn)里程碑突破。公司自主研發(fā)的全球創(chuàng)新靶向成纖維細(xì)胞活化蛋白(FAP)的小分子RDC藥物GPN01530獲FDA批準(zhǔn)開展I/II期臨床��,成為公司頭款獲FDA批準(zhǔn)臨床的自研RDC產(chǎn)品,其臨床獲批也為公司核藥產(chǎn)品管線的國際化開發(fā)提供了重要范式�,同時也展現(xiàn)出了遠(yuǎn)大醫(yī)藥核藥技術(shù)平臺優(yōu)異的臨床前開發(fā)及國際注冊能力;GPN02006早前在中國開展的研究者發(fā)起的臨床研究(IIT臨床研究)取得了里程碑式突破�,并在2025年北美核醫(yī)學(xué)與分子影像學(xué)會(SNMMI)年會斬獲口頭報告,有望成為頭個靶向GPC-3的肝細(xì)胞癌診斷RDC產(chǎn)品����,全球化創(chuàng)新實力持續(xù)彰顯。
在產(chǎn)業(yè)基礎(chǔ)建設(shè)方面�����,公司核藥產(chǎn)業(yè)也已實現(xiàn)全面自主可控能力�。2025年6月,遠(yuǎn)大醫(yī)藥成都溫江放射性藥物研發(fā)及生產(chǎn)基地正式投運��,為頭個核藥全產(chǎn)業(yè)鏈閉環(huán)平臺���。該基地?fù)碛?4條GMP高標(biāo)準(zhǔn)生產(chǎn)線��,實現(xiàn)同位素制備���、研發(fā)、生產(chǎn)��、臨床及商業(yè)化全鏈條自主可控,破解核藥關(guān)鍵環(huán)節(jié)“卡脖子”問題�。該基地是目前國際上核素種類全、自動化程度高的智能核藥工廠之一�,為公司全球創(chuàng)新成果快速產(chǎn)業(yè)化提供堅實支撐。
此次釔[90Y]微球注射液成功達(dá)到海外臨床試驗終點����,是遠(yuǎn)大醫(yī)藥“Go Global”戰(zhàn)略的里程碑進(jìn)展�,進(jìn)一步彰顯了公司強大的國際化研發(fā)能力,同時也體現(xiàn)了公司核藥平臺的巨大潛力�����。未來����,遠(yuǎn)大醫(yī)藥有望持續(xù)加強在核藥領(lǐng)域的全球競爭優(yōu)勢,加速推進(jìn)更多創(chuàng)新核藥的研發(fā)與轉(zhuǎn)化����,為攻克更多惡性腫瘤、改善患者生存質(zhì)量貢獻(xiàn)力量��,并持續(xù)鞏固其在全球核藥賽道的企業(yè)地位��。





評論